Làm sao để nhớ hóa trị của nguyên tử? Cách học thuộc hóa trị lớp 8 dễ dàng cách học hóa trị dễ nhớ. Làm sao để có thể học hóa trị một cách nhanh nhất nhưng lại nhớ lâu nhất. 60s.edu.vn sẽ chia sẻ bí quyết học thuộc qua bài ca hóa trị, được truyền cho rất nhiều thế hệ học sinh.
I. Cách học thuộc hóa trị lớp 8 dễ dàng
Hóa trị là của một nguyên tố được xác định bằng số liên kết hóa học một nguyên tử của nguyên tố đó tạo nên trong phân tử. Hóa trị của nguyên tố trong hợp chất ion là điện hóa trị, có giá trị bằng điện tích của ion tạo thành từ nguyên tố đó.
1. Cách học thuộc hóa trị lớp 8
Hóa trị I: Hg , Ag , Na , Cl , K , Li. Đọc là: Hết Bạc Na Lo Kiếm Liền
Hóa trị II: Mg , Ca , Ba , Pb . Cu , Hg , Fe, Zn – đọc là: Má Cản Ba Phá Cửa Hàng Sắt Kẽm
Hóa trị III: có Al và Fe
Hóa trị I là: Na, K, Ag, Cl.
Hóa trị III là: Al, Fe
Hóa trị II: còn lại (với Fe có hóa trị II và III luôn).
Hoặc là học câu nói vui sau : hai Bà Cả không Mua Chì Kẽm Sắt Cũng Mãi một Năm Ăn hết Khoảng ba Phen Vàng Nhưng Sắt Nhôm năm Phen bốn Chỉ
Cách học thuộc hóa trị của nguyên tố dễ dàng thì học sinh nên lấy những hợp chất của oxi để làm ví dụ sau đó xác định hóa trị của các nguyên tố khác.
Ví dụ cụ thể: Để xác định hóa trị của Fe và Na ta có thể lấy những oxit như Na2O, FeO, Fe2O3.
Ta làm như sau:
Ta biết nguyên tố Oxi luôn luôn có hóa trị II
x II
Na2 O
Na2O sau khi viền xong rồi ta áp dụng công thức sau:
x II
a b
Ax = By
a.x b.y
Na2 O x.2
x II
II .1 (ở đây ta xem số La Ma như số thường và nhân chia như bình thường nhé)
Na2 O x.2
II .1 2.x 2
x 1.
Vây hóa tri của Na : I
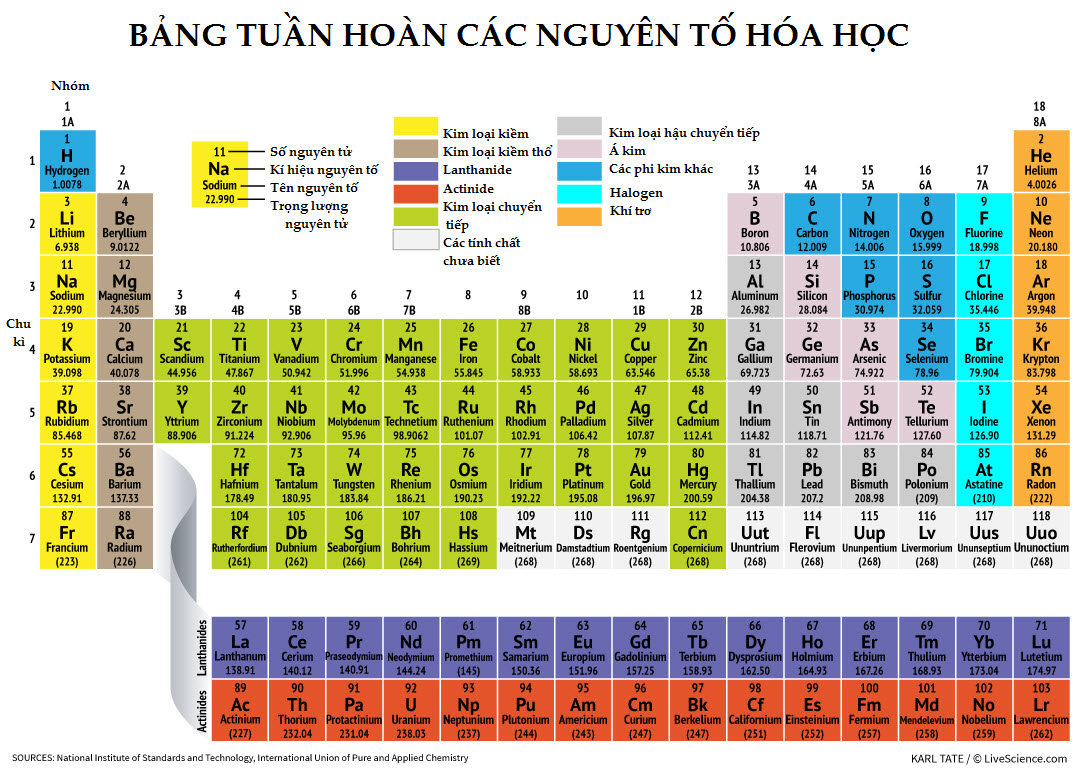
2. Cách học thuộc hóa trị lớp 8 theo số hóa trị của nguyên tố
Chúng ta nên nhớ là hóa trị phải ghi bằng chữ số La Mã. Tương tự như vậy đối với các hợp chất khác.
Hóa trị thì học theo nhóm cho dễ:
Nhóm có 1 hóa trị:
Bao gồm nhóm hóa trị I, II, III, IV
Hóa trị I bao gồm: H, Li, F, Na, Cl, K, Ag, Br
Hóa trị II bao gồm: Be, O, Mg, Ca, Zn, Ba, Hg
Hóa trị III bao gồm: B, Al
Hóa trị IV bao gồm: Si
Nhóm có nhiều hóa trị bao gồm:
Cacbon: IV, II
Chì: II, IV
Crom: III, II
Nito: III, II, IV
Photpho: III, V
Lưu huỳnh: IV, II, VI
Mangan: IV, II, VII…….Các hóa trị in đậm thường sử dụng nhiều nhất trong khi học.
Có 5 nhóm cần thuộc hóa trị bảng trang 42 SGK hóa học 8 các em cần học thuộc
Hóa trị của các gốc gồm nhiều nguyên tố hóa học:
Các gốc hóa trị I gồm :OH (hidroxit ), NO3 ( nitrat )
Các gốc hóa trị II gồm: CO3 ( cacbonat ), SO4 ( sunfat )
Các gốc hóa trị III gồm : PO4 ( photphat )
3. Cách học thuộc hóa trị lớp 8 theo bài ca hóa trị
Ngoài ra còn có bài thơ hóa trị cho nhanh-gọn-nhẹ :
Kali (K), iốt (I) Hidrô (H)
Natri với bạc (Ag) , clo (Cl) một loài
Là hoá trị ( I ) hỡi ai,
Nhớ ghi cho kỹ khỏi hoài phân vân.
Magiê (Mg) , kẽm với thuỷ ngân (Hg),
Ôxi (O) , đồng(Cu), thiếc (Sn) thêm phần bari
Cuối cùng thêm chú canxi ,
Hoá trị II nhớ có gì khó khăn .
Này nhôm hoá trị III lần
In sâu trí nhớ khi cần có luôn .
Cacbon ,silic(Si) này đây,
Có hoá trị IV không ngày nào quên.
Sắt kia lắm lúc hay phiền,
II , III nhớ liền nhau thôi.
Lại gặp nitơ khổ rồi
I , II , III , IV khi thời lên V
Lưu huỳnh lắm lúc chơi khăm
Xuống II lên VI khi nằm thứ IV
Phốt pho nói đến không dư
Có ai hỏi đến thì ừ rằng V
Em ơi gắng học chăm
Bài ca hoá trị cả năm cần dùng.

II. Bài tập áp dụng luyện tập cách học thuộc hóa trị lớp 8
1. Bài tập áp dụng luyện tập cách học thuộc hóa trị lớp 8
Bài tập tìm công thức hóa học của hợp chất biết hóa trị
B1: Viết Công thức hóa học chung
B2: Theo quy tắc hóa trị:
a.x = b.y
=>Tìm giá trị của chỉ số
Chọn x = b’; y = a’, suy ra Công thức hóa học đúng.
Chú ý: Nếu một nhóm nguyên tử thì phải xem như một nguyên tố và lập Công thức hóa học như một nguyên tố khác.
Khi viết hóa trị phải viết theo số La Mã, còn chỉ số là số tự nhiên.
Yêu cầu: Để lập được CTHH của hợp chất bắt buộc nắm chắc kí hiệu hóa học và hóa trị của các nguyên tố tạo nên hợp chất đó.
* Hoặc nhớ mẹo hóa trị một số nguyên tố thường gặp như sau:
Hóa trị I là: K Na Ag H Br Cl
Khi Nàng Ăn Hắn Bỏ Chạy
Hóa trị II là: O Ba Ca Mg Zn Fe Cu
Ông Ba Cần May Zap Sắt Đồng
Hóa trị III là: Al Fe
Anh Fap
Đối với nguyên tố có nhiều hóa trị thì đề sẽ cho hóa trị ta chỉ làm theo thôi.
Ví dụ 1
Lập Công thức hóa học của hợp chất:
a) Nhôm oxit được tạo nên tử 2 nguyên tố oxi và nhôm Al
Lời Giải
Theo quy tắc hóa trị ta có:
x . III = y . II
=> x = 2; y = 3
Vậy Công thức hóa học: Al2O3
b) Cacbon đioxit gồm C(IV) và O (II)
Lời Giải
Theo quy tắc hóa trị ta có:
x . IV = y . II
=> x = 1; y = 2
Vậy Công thức hóa học: CO2
b) Natri photphat gồm Na (I) và PO4(III)
Giải
Theo quy tắc hóa trị ta có:
x . I = y . III
=> x = 3; y = 1
Vậy Công thức hóa học : Na3PO4
Viết Công thức hóa học hoặc lập nhanh Công thức hóa học: không cần làm theo từng bước cụ thể như trên, mà chỉ cần nắm rõ quy tắc chéo: hóa trị của nguyên tố này sẽ là chỉ số của nguyên tố kia và ngược lại (với điều kiện rằng các tỉ số phải tối giản trước).
Chú ý: Nếu hai nguyên tố cùng hóa trị thì không cần ghi chỉ số ( mặc định là 1 rồi)
Ví dụ
1) Viết công thức hóa học của hợp chất tạo bởi S (VI) và O.
=> Công thức hóa học SO3
(Do VI / II = 3/1 nên chéo xuống chỉ số của S là 1 còn O là 3).
2) Viết công thức hóa học của Fe(III) và SO4 hóa trị (II)
Công thức hóa học Fe2(SO4)3
(Lí giải: Tỉ lệ hóa trị III và II không cần tối giản, hóa trị III của Fe trở thành chỉ số 3 của SO4, như vậy phải đóng ngoặc nhóm SO4, hiểu là có 3 nhóm SO4. Hóa trị II của SO4 trở thành chỉ số 2 của Fe.)
Chú ý: khi đã thành thạo, nắm rõ quy tác chúng ta có thể không cần viết hóa trị lên trên đỉnh nguyên tố, nhóm nguyên tử.

2. Bài tập áp dụng luyện tập cách học thuộc hóa trị lớp 8( Kèm lời giải)
a, Bài tập
Bài tập 1
Lập công thức hóa học của các hợp chất với hidro của các nguyên tố dưới đây:
a) N (III) b) C (IV) c) S (II) d) Cl
Chú ý: a, b viết H đứng sau nguyên tố N, C.
c, d viết H đứng trước nguyên tố S và Cl.
Bài tập 2
Lập công thức hóa học cho các hợp chất:
a. Cu(II) và Cl
d. NH4 (I) và SO4
b. Al và NO3
c. Ca và PO4
e. Mg và O
g. Fe( III ) và SO4
Bài tập 3
Lập công thức hóa học của các hợp chất:
1. Al và PO4 2. Na và SO4 3. Fe (II) và Cl
4. Mg và CO3 5. Hg (II) và NO3 6. Zn và Br
7. K và SO3 8. Na và Cl 9. Na và PO4
10.Ba và HCO3(I) 11.K và H2PO4(I) 12.Na và HSO4(I)
Bài tập 4
Lập công thức hóa học hợp chất.
1/Lập CTHH hợp chất tạo bởi nhóm NO3 và nguyên tố Al. Cho biết ý nghĩa CTHH trên.
2/ Lập CTHH hợp chất phân tử gồm:Ba và SO4. Cho biết ý nghĩa CTHH trên.
3/Lập CTHH hợp chất có phân tử gồm nguyên tố Mg và nhóm OH. Cho biết ý nghĩa CTHH trên.
Bài tập 5
Viết CTHH của các hợp chất với lưu huỳnh (II) của các nguyên tố sau đây:
a) K (I) b) Fe (II) c) Al (III) d) Hg (II)
Bài tập 6
Viết CTHH và tính phân tử khối của các hợp chất sau:
a) Điphotpho pentaoxit gồm P(V) và O.
b) Axit sunfuric gồm H và SO4.
c) Bari cacbonat gồm Ba và CO3.
d) Canxi photphat gồm Ca và PO4.
Bài 8 (*)
Xét các CTHH: Z(NO3)3; (NH4)3T; X2SO4; H2Y; . Biết hóa trị của SO4 là II, NH4 (I), NO3(I). Viết CTHH của hợp chất gồm:
a) X và H b) Z và SO4 c) T và H d) X và Y
e) X và T f) Y và Z g) Z và T.
Bài 9 (*)
Cho 2 chất có CTHH là A2S và B2O3. CTHH của hợp chất tạo bởi A và B là ?
b, Hướng dẫn
Bài 1
Đáp số
a) NH3 b) CH4 c) H2S d) HCl
Bài 2
Đáp số
a) CuCl2 b) Al(NO3)3 c) Ca3(PO4)2 d) (NH4)2SO4
e) MgO f) Fe2(SO4)3
Bài 3
Đáp số
1. AlPO4 2. Na2SO4 3. FeCl2
4. K2SO3 5. NaCl 6. Na3PO4
7. MgCO3 8. Hg(NO3)2 9. ZnBr2
10. Ba(HCO3)2 11. KH2PO4 12. NaHSO4
Bài 4
Đáp số
1/ Al(NO3)3
– Tạo bởi 3 nguyên tố Al, N, O.
– Gồm 1Al, 3N, 9O.
– PTK = 27 + 3 . 14 + 9 . 16 = 213.
3/ Mg(OH)2
– Tạo bởi 3 nguyên tố Mg, O, H.
– Gồm 1Mg, 2O, 2H.|
– PTK = 24 + 2 . 16 + 2 . 1 = 58.
2/ BaSO4
– Tạo bởi 3 nguyên tố Ba, S và O.
– Gồm 1 Ba, 1S, 4O.
– PTK = 137 + 32 + 4 . 16 = 233.
Bài 5
Đáp số
a) K2S b) HgS c) Al2S3 d) FeS.
Bài 6
Đáp số
a) P2O5 = 142.
b) Ca3(PO4)2 = 310.
c) H2SO4 = 98.
d) BaCO3 = 197.
Bài 8 (*)
Đáp số
a) XH3 b) Z2(SO4)3 c) TH3 d) XY
e) X3T2 f) Y3Z2 g) XT
Bài 9 (*)
Đáp số: A3B
Trên đây là hướng dẫn chi tiết cách học thuộc hóa trị lớp 8 và bài tập, lời giải chi tiết, mong rằng có ích đối với các em trong việc học hóa học tốt hơn.