Bài tập este là dạng bài tập xuất hiện nhiều trong các bài kiểm tra, đề thi và đặc biệt là trong đề thi đại học. Chính vì vậy bạn cần chú ý nắm vững lý thuyết cũng như cách giải của dạng bài tập này để có thể làm bài tốt. Một số bài tập este có lời giải chắc chắn sẽ giúp ích cho bạn trong việc ôn tập đấy!
1. Lý thuyết cần chú ý cho bài tập este
Để làm tốt bài tập este hay bất cứ dạng bài tập nào trước tiên bạn cần nắm chắc được lý thuyết của dạng bài tập đó. Đối với lý thuyết bài tập este bạn cần lưu ý các điều sau:
1.1. Khái niệm este
Phương trình hóa học của phản ứng este:
CH3COOH + HOC2H5—> CH3COOC2H5 + H2O ( CH3COOC2H5 chính là este)
Từ phương trình hóa học trên ta có thể thấy Este nó là sản phẩm thay thế của nhóm -OH của nhóm axit cacboxylic bằng nhóm OR’ ( R ở đây là gốc hidrocacbon)
Ta có công thức chung của este là:

1.2. Tính chất hóa học của este
Bạn cần nhớ rằng trong este trung tâm phản ứng chính là nhóm chức COO
– Các phản ứng thủy phân của este:
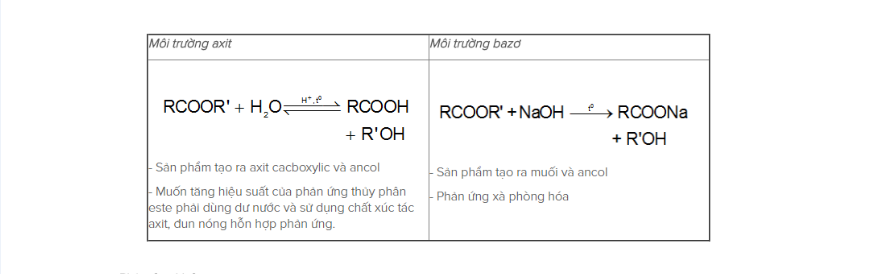
– Phản ứng khác của este:

1.3. Dấu hiệu nhận biết este
Cần nắm rõ được các dấu hiệu nhận biết este mới có thể làm bài tập este một cách trôi chảy được. Este có các dấu hiệu nhận biết như sau:
– Este không no có phản ứng làm mất màu dung dịch Brom
– Các este của ancol không bền sẽ bị thủy phân tạo andehit có khả năng tráng gương
– Este của axit fomic có khả năng tráng gương
– Este của glixerol hoặc chất béo khi thủy phân cho ra sản phẩm hòa tan Cu(OH)2
2. Bài tập este có lời giải
2.1. Bài tập este
Bài tập 1: Đem đốt cháy 6g este X thu được 4,48 l CO2 (đktc) và 3,6g H2O. Tìm CTCT của X.
Bài tâp 2: Đem đốt cháy một lượng hỗn hợp hai este no, đơn chức cần 3,976 lit O2 (đktc) thu được 6,38g CO2 (đốt cháy hoàn toàn). Tiếp theo cho lượng este này tác dụng vừa đủ với KOH thu được hỗn hợp gồm 2 ancol kế tiếp nhau và 3,92g muối của một axit hữu cơ. Hãy tìm CTCT 2 este đó.
Bài tập 3: Cho hỗn hợp 14,8g gồm 2 este đồng phân của nhau bay hơi trong điều kiện thích hợp. Thu được một thể tích hơi đúng bằng thể tích của 6,4g oxi cũng trong cùng điều kiện trên. Nếu đốt cháy hoàn toàn hỗn hợp hai este trên ta thu được sản phẩm phản ứng là CO2 và H2O. Biết rằng tỉ lệ thể tích khí CO2 và hơi H2O là 1:1, hãy xác định CTCT của 2 este.
2.2. Lời giải bải tập este
Bài 1:
nCO2 = 0,2 mol
nH2O = 0,2 mol
=> nCO2 = nH2O => este Y no, đơn chức, mạch hở
Đặt CTTQ của Y là CnH2nO2
Ta có: CnH2nO2 + O2 ———–> nCO2 + nH2O
14n+32 n mol
6 0,2 mol
=> (14n +32).0,2 = 6n
=> n = 2
=> CTPT của X: C2H4O2
=> CTCT của X: HCOOCH3
Bài tập 2:
nO2 = 0,1775 mol
nCO2 = 0,145 mol
2 este + KOH => hỗn hợp 2 ancol kế tiếp và muối của 1 axit hữu cơ => Bài toán 2 este tạo bởi cùng 1 axit hữu cơ và 2 ancol là đồng đẳng liên tiếp.
Đặt CTPT trung bình của 2 este là C{_{\bar{n}}}H_{2\bar{n}}O_{2}
Phản ứng cháy:
CnH2nO2 + ((3n-2)/2) O2 ——–> nCO2+ nH2O (n ở đây là n trung bình)
Ta có: ((3n-2)/2) : n <—> 0,1775: 0,145
=> n = 3,625
=> CTPT của 2 este là C3H6O2 và C4H8O2
số mol este : neste = \frac{3}{2}nCO2- nO2 = 0,04 mol
Phản ứng thủy phân: Đặt CTTQ của 2 este là RCOO\bar{{R}’}
=> Thủy phân thu được muối RCOOK
nRCOOK = neste = 0,04 mol
=> MRCOOK = \frac{3,92}{0,04} = 98
=> R =15: CH3-
Vậy: CTCT của 2 este là: CH3COOCH3 và CH3COOC2H5.
Bài tập 3:
Theo bài ra: nCO2 : nH2O = 1:1 => 2 este là no, đơn chức, mạch hở
Đặt CTTQ của 2 este đồng phân là CnH2nO2, n>=2
Có: thể tích hơi của 14,8g este bằng thể tích hơi của 6,4g O2
=> neste = nO2 = 0,2 mol
=> Meste = 74
=> 14n+32 =74 => n=3=>CTPT: C3H6O2
CTCT của 2 este là CH3COOCH3 và HCOOC2H5.
Để có thể làm tốt nhất dạng bài tập este bạn cần ôn luyện nhiều để ” ngấm” sâu vào đầu. Trong quá trình làm bài ôn luyện cũng nên làm cẩn thận, sau đó khi quen và thành thạo mới giải nhanh. Một số bài tập este có lời giải chắc chắn sẽ rất hữu ích cho bạn, chúc các bạn học tốt!











