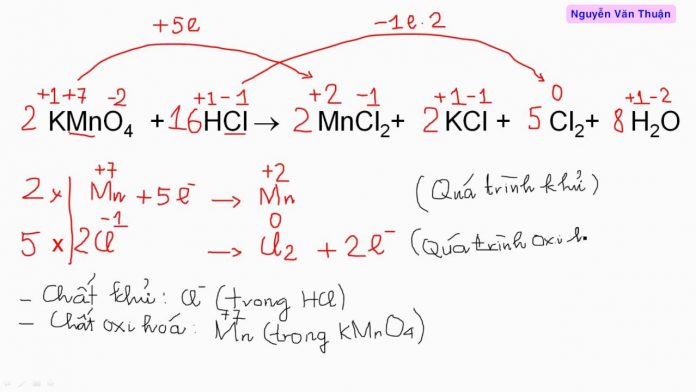
Cách cân bằng phản ứng oxi hóa khử nhanh nhất có lẽ luôn là vấn đề mà các bạn học sinh lưu tâm nhất. Để cân bằng phản ứng không chỉ cần sự tỉ mỉ, tư duy mà cần cả một số mẹo. Sau đây, 60s.edu.vn xin chia sẻ phương pháp làm bài hiệu quả nhất.
I. Nội dung cách cân bằng phản ứng oxi hóa khử
1. Cách cân bằng phản ứng oxi hóa khử nhanh nhất
Nội dung 1: Số oxi hoá, phương pháp tính số oxi hóa của nguyên tố trong các hợp chất hóa học
Số oxi hóa của một nguyên tố trong phân tử là số điện tích của nguyên tử đó trong công thức hóa học, tức hiểu rằng liên kết giữa các nguyên tử nguyên tố trong phân tử là liên kết ion.
Quy tắc xác định số oxi hóa của các chất:
• Trong đơn chất, số oxi hóa nguyên tố là 0.
• Tổng các số oxi hoá của các nguyên tử trong công thức phân tử (trung hoà điện) bằng 0.
• Tổng các số oxi hoá của các nguyên tử nguyên tố trong một ion phức tạp bằng điện tích của ion đó.
• Khi tham gia vào phân tử, số oxi hoá của 2 nguyên tố cơ bản có trị số không đổi: H là +1, O là -2 …
Lưu ý: Dấu của số oxi hoá đặt trước con số, và dấu của điện tích ion đặt sau con số (số oxi hóa Fe+3 ; Ion sắt (III) ghi: Fe3+. Đây là lưu ý quan trọng trong cân bằng phản ứng oxi hóa khử.

Nội dung 2: Các phương pháp cân bằng phản ứng oxi hoá khử
Phương pháp 1: Phương pháp cân bằng đại số đơn giản
Nguyên tắc khi cân bằng:
Số nguyên tử của mỗi nguyên tố nằm ở hai vế luôn bằng nhau.
Quy trình cân bằng:
Đặt ẩn số là các hệ số hợp thức. Dùng định luật bảo toàn khối lượng để cân bằng nguyên tố và lập phương trình đại số.
Ví dụ: a FeS2 + b O2→ c Fe2O3 + d SO2
Ta có: Fe : a = 2c
S : 2a = d
O : 2b = 3c + 2d
Chọn c = 1 thì a=2, d=4, b = 11/2
Nhân tất cả hai vế với 2 ta được phương trình mới
4FeS2 + 11O2 → 2Fe2O3 + 8SO2
Phương pháp 2: Sử dụng theo phương pháp cân bằng electron
Nguyên tắc: dựa vào sự bảo toàn số electron nghĩa là tổng số electron của chất khử cho luôn luôn bằng tổng số electron chất oxi hóa nhận.

Các bước cân bằng cân bằng phản ứng oxi hoá khử
Bước 1: hoàn thành sơ đồ phản ứng với các nguyên tố có sự thay đổi số oxi hóa.
Bước 2: Hoàn thiện các quá trình: khử (cho electron), oxi hóa (nhận electron).
Bước 3:Cân bằng electron: nhân hệ số để:
Tổng số electron cho = tổng số electron nhận.
(tổng số oxi hóa giảm = tổng số oxi hóa tăng).
Bước 4: Cân bằng nguyên tố không thay đổi số oxi hoá :
kim loại (ion dương):
gốc axit (ion âm).
môi trường (axit, bazơ).
nước (cân bằng H2O để cân bằng hiđro).
Bước 5: Kiểm soát số nguyên tử oxi ở 2 vế (phải bằng nhau).
Ví dụ:
Fe + H2SO4đặc nóng → Fe2(SO4)3 + SO2 + H2O
Fe0 → Fe+3 + 3e
1 x 2Fe0 → 2Fe+3 + 6e
3 x S+6 + 2e → S+4
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2 + 6H20
Phương pháp số 3: phương pháp cân bằng phương trình oxi hóa khử theo ion – electron:
Đối tượng áp dụng: sử dụng trong các quá trình diễn ra trong các dung dịch, có sự xuất hiện của môi trường (H2O, dung dịch axit, bazơ tham gia).
Các nguyên tắc cơ bản áp dụng:
•Trường hợp phản ứng có axit tham gia: bên nào của phương trình thừa O phải thêm H+ để tạo H2O và ngược lại.
•Trường hợp phản ứng có bazơ tham gia: bên nào của phương trình thừa O phải thêm H2O để tạo ra OH-
Các bước tiến hành:
Bước 1: Tách các ion, tính số các nguyên tố có số oxi hóa thay đổi sau đó viết các nửa phản ứng oxi hóa – khử.
Bước 2: Cân bằng các bán phản ứng:
Cân bằng số nguyên tử của nguyên tố ở hai vế trong phương trình
Thêm H+ hoặc OH-
Thêm H2O để làm đảm bảo cân bằng số nguyên tử H
Tính toán sao cho số nguyên tử oxi ở 2 vế phải cân bằng.
Tiếp theo là cân bằng điện tích: thêm electron vào mỗi nửa phản ứng để cân bằng điện tích trong phương trình
Bước 3: Cân bằng electron: tiến hành nhân hệ số để:
Tổng số electron cho = tổng số electron nhận.
(tổng số oxi hóa giảm = tổng số oxi hóa tăng).
Bước 4: Cộng tổng các nửa phản ứng ta có phương trình ion thu gọn.
Bước 5: Để chuyển phương trình dạng ion thu gọn thành phương trình ion đầy đủ và phương trình phân tử cần cộng vào 2 vế những lượng bằng nhau các cation hoặc anion để bù trừ điện tích ta cân bằng được phản ứng oxi hóa khử.
2. Ví dụ cụ thể
Ví dụ: Cân bằng phương trình phản ứng:
Cu + HNO3 → Cu(NO3)2 + NO + H2O
Bước 1: Cu + H+ + NO3- → Cu2+ + 2NO3- + NO + H2O
Cu0 → Cu2+
NO3-→ NO
Bước 2: Cân bằng nguyên tố:
Cu → Cu2+
NO3- + 4H+ → NO + 2H2O
Cân bằng điện tích
Cu → Cu2+ + 2e
NO3- + 4H+ + 3e → NO + 2H2O
Bước 3: Cân bằng electron:
3 x Cu → Cu2+ + 2
2 x NO3- + 4H+ + 3e → NO + 2H2O
Bước 4: 3Cu + 2NO3- + 8H+ → 3Cu2+ + 2NO + 4H2O
Bước 5: 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO +4H2O